Rede Sentinela: Anvisa publica novos alertas de farmacovigilância: A Gerência de Farmacovigilância da Anvisa (GFARM) publicou, recentemente, três alertas referentes à segurança dos pacientes e usuários de medicamentos.
O primeiro deles se refere ao risco de embolia gasosa associado ao uso
de selantes contendo fibrinogênio administrados por pulverização (spray)
quarta-feira, 29 de janeiro de 2014
terça-feira, 28 de janeiro de 2014
Resolução 357 / 2001 - Da prestação de assistência farmacêutica domiciliar
Art. 97 - A prestação da assistência farmacêutica domiciliar no estrito cumprimento da legislação vigente, dos princípios éticos da profissão farmacêutica e dos requisitosmínimos contemplados neste regulamento deve atender a melhoria do acesso dos pacientes e da população em geral aos cuidados farmacêuticos.
Parágrafo único - A prestação da assistência farmacêutica domiciliar somente é permitida em farmácias e drogarias, abertas ao público, definidas nos termos da lei federal nº 5991 de 17 de dezembro de 1973
Seção I
Dos Princípios Gerais
Art. 98 - A ação do farmacêutico deve pautar-se pelos princípios éticos que regem o seu exercício profissional especialmente à propaganda, publicidade, promoção de medicamentos, a relação com o paciente, colegas e outros profissionais de saúde.
Art. 99 - Deve ser assegurado o princípio da livre escolha da farmácia e do farmacêutico pelo usuário.
Art. 100 - Cabe ao farmacêutico diretor técnico a garantia do cumprimento da legislação em vigor, das normas éticas dentro e fora da farmácia no estrito cumprimento dos atos inerentes ao farmacêutico e com vista a adequar a qualidade do serviço com as necessidades do paciente.
Art. 101 - A prestação deste serviço por parte do farmacêutico na farmácia e drogaria é facultativo.
Art. 102 - O farmacêutico diretor técnico pela farmácia prestadora de assistência farmacêutica domiciliar deve articular-se com outros colegas no sentido de proporcionara melhor assistência possível ao atendimento dos usuários.
Art. 103 - As informações e condições da prestação desta assistência deve ser dada à população tendo em atenção os princípios gerais e as normas específicas estipuladas de forma a não afetar a dignidade profissional dos farmacêuticos.
Art. 104 - A remuneração da prestação desta assistência é obrigatória.
Seção II
Das Normas Específicas
Art. 105 - É assegurada a prestação dos serviços farmacêuticos domiciliar quando da solicitação através dos meios de comunicação existentes, sejam estes fax, telefone,correio, Internet ou similares, desde que comprovado pelo estabelecimento farmacêutico e farmacêutico diretor técnico, o cadastro prévio do beneficiário, o qual deverá ser disponibilizado às autoridades de fiscalização, em qualquer tempo.
Parágrafo único - É obrigatório o prévio cadastramento por parte do usuário da assistência farmacêutica domiciliar, cabendo aos Conselhos Regionais de Farmácia expedirem deliberações necessárias a elaboração do cadastro mencionado neste artigo,cujo procedimento é de obrigação do farmacêutico diretor técnico ou substituto.
Art. 106 - O farmacêutico deverá manter na farmácia toda a informação necessária: identificação do paciente, identificação do prescritor, prescrição, produtos dispensados, características particulares do paciente e patologias. Caso não seja possível dispor de toda informação especificamente da prescrição deverá o farmacêutico de acordo com o paciente, encontrar uma forma de avaliação e acompanhamento.
Art. 107 - O farmacêutico é responsável pela validação da informação recebida, solicitando ao usuário ou ao prescritor os esclarecimentos adicionais necessárias à dispensação dos medicamentos.
Art. 108 - Os produtos a serem dispensados devem ser acondicionados em embalagens seladas e individualizadas por usuário de acordo com a características dos produtos requeridos. Deve ainda constar todas as informações necessárias para a sua correta utilização.
Art. 109 - O transporte dos medicamentos deverá assegurar que os produtos chegarão aos usuários em perfeitas condições de conservação e segurança, tendo para qual que cumprir as adequadas condições de temperatura, luminosidade e umidade de acordo com as definições da Farmacopéia brasileira ou de outras normas determinados pela ANVISA.
Art. 110 - A dispensação de medicamentos domiciliar será acompanhada por documento onde deverão constar as seguintes informações: nome do usuário, residência do usuário, nome da farmácia, nome do farmacêutico, meio de contato, endereço da farmácia e a descrição dos produtos dispensados.
Art. 111- O usuário deverá conferir os produtos solicitados, bem como as informações que devem acompanha-los. Em caso de dúvida deve se reportar ao farmacêutico.
Parágrafo único - No caso de não haver contato por parte do usuário, deverá o farmacêutico obrigatoriamente entrar em contato com o mesmo, para averiguação de eventuais dúvidas na utilização dos produtos dispensados.
Art. 112 - Fica vedada a dispensação de medicamentos domiciliar fora de suas embalagens originais.
Art. 113 - Para medicamentos manipulados o farmacêutico deverá dispensar em embalagens com lacre ou outro mecanismo que assegure a inviolabilidade do conteúdo.
Art. 114 - Os registros decorrente da prestação de assistência farmacêutica domiciliar devem ser elaboradas com o prévio consentimento por expresso dos usuários e respeitando a sua privacidade. (Anexo II)
I. A confidencialidade dos dados, a privacidade do paciente e a garantia de que acessos indevidos ou não autorizados a estes dados sejam evitados e que seu sigilo seja garantido;
II. Que os dados sobre pacientes, armazenados em formato eletrônico, não serão utilizados para qualquer forma de promoção, publicidade, propaganda ou outra forma de indução de consumo de medicamentos
Fonte: Resolução 357/01 CFF
Hora Extra - O que diz a Lei Trabalhista (CLT)
HORAS EXTRAS
A legislação
trabalhista vigente estabelece que a duração normal do trabalho, salvo os casos
especiais, é de 8 (oito) horas diárias e 44 (quarenta e quatro) semanais, no
máximo.
Todavia,
poderá a jornada diária de trabalho dos empregados maiores ser acrescida de
horas suplementares, em número não excedentes a duas, no máximo, para efeito de
serviço extraordinário, mediante acordo individual, acordo coletivo,
convenção
coletiva ou sentença normativa. Excepcionalmente, ocorrendo necessidade
imperiosa, poderá ser prorrogada além do limite legalmente permitido.
REMUNERAÇÃO DO
SERVIÇO EXTRAORDINÁRIO
A remuneração
do serviço extraordinário, desde a promulgação da Constituição Federal/1988, que
deverá constar, obrigatoriamente, do acordo, convenção ou sentença normativa,
será, no mínimo, 50% (cinquenta por cento) superior à da hora normal.
Enunciado nº
264, do TST:
"A remuneração do serviço suplementar é composto do...
TRABALHO DA
MULHER
Tendo a
Constituição Federal disposto que todos são iguais perante a lei e que não deve
haver distinção de qualquer natureza, e que homens e mulheres são iguais em
direito e obrigações, aplica-se à mulher maior de idade, no que diz respeito ao
serviço extraordinário, o mesmo tratamento dispensado ao homem.
TRABALHO DE MENOR
A prestação
de serviço extraordinário pelo empregado menor somente é permitida em caso
excepcional, por motivo de força maior e desde que o
trabalho do menor seja
imprescindível ao funcionamento do estabelecimento.
NECESSIDADE
IMPERIOSA
Ocorrendo
necessidade imperiosa, por motivo de força maior, realização ou conclusão de
serviços inadiáveis cuja inexecução possa acarretar prejuízo manifesto, a
duração do trabalho poderá exceder ao limite legal ou convencionado,
independentemente de acordo ou contrato coletivo, devendo, contudo, ser
comunicado à Delegacia Regional do Trabalho no prazo de 10 (dez) dias no caso de
empregados maiores e 48 (quarenta e oito) horas no caso de empregados
menores.
SERVIÇO
EXTERNO
Os empregados
que prestam serviços externos incompatíveis com a fixação de horário, com
registro de tal condição na
CTPS e na ficha ou livro de registro de empregados,
não têm direito a horas extras.
CARGO DE
CONFIANÇA - GERENTE
Os
gerentes,
assim considerados os exercentes de cargos de gestão, aos quais se equiparam os
diretores e chefes de departamentos ou filial, não fazem jus à remuneração pelo
serviço extraordinário, pois não lhes aplicam as normas relativas à duração
normal do trabalho.
Fonte: Guia Trabalhista
Deu no G1: “Santarém já conta com assistência integral farmacêutica”, diz CRF
Superintendente do Conselho de Farmácia diz que município é exemplo.
Lei exige que farmácias e drogarias tenham farmacêutico em tempo integral
A Superintendência do Conselho Regional de Farmácia em Santarém, oeste do Pará, informou, nesta semana, que todas as farmácias e drogarias do município contam com a assistência de farmacêutico durante todo o expediente. No país inteiro, 35% dos mais de 76 mil estabelecimentos não têm o profissional em tempo integral.
“Santarém, hoje, já conta com assistência integral farmacêutica. Ou seja, enquanto a farmácia estiver aberta, é obrigatória a presença de um profissional farmacêutico”, revela o Superintendente do Conselho Regional de Farmácia, Marcos Castelo.
Ele conta que as fiscalizações têm sido intensificadas, acontecendo em diferentes horários, atestando que, de fato, farmácias e drogarias possuem farmacêutico. “O fiscal cumpre determinada rota, que é sorteada para aquele dia. E aí ele tem um número ‘x’ de estabelecimentos farmacêuticos dos quais ele vai fiscalizar rotineiramente. Ou seja, ele pode ir duas, três, ou até quatro vezes no mesmo estabelecimento no mesmo mês, em horários diferentes”, explica Castelo.
O farmacêutico tem importante atuação. Ele pode desenvolver pesquisas de novos medicamentos e testes e aplicação de drogas, na área industrial, e controlar e indicar a venda de remédios em farmácias, drogarias e hospitais, no setor comercial.
“É uma forma de atenção, mesmo. É um esclarecimento, as pessoas têm dúvida, às vezes não têm acesso ao médico. Então realizamos este trabalho na farmácia. E isso causa uma segurança para o tratamento do paciente”, esclarece a farmacêutica Suzane Fernandes.
Fiscalizações
No entanto, o Conselho Regional de Farmácia havia constatado, durante fiscalizações realizadas em 2013, que 10% das farmácias e drogarias de Santarém não obedeciam a lei que determina a presença de um farmacêutico de plantão durante todo o período em que o estabelecimento esteja de portas abertas. Foram feitas mais de 20 operações de fiscalização. Das 140 drogarias existentes no município, em 14 unidades esses profissionais não foram encontrados no momento da vistoria.
Fonte: G1
terça-feira, 21 de janeiro de 2014
Deputados criticam proposta que exime drogarias de ter farmacêutico
Foto: Gustavo Lima Alice Portugal ressalta que farmácia não é qualquer comércio e tem que ter assistência à população
Alice Portugal ressalta que farmácia não é qualquer comércio e tem que ter assistência à população
 Alice Portugal ressalta que farmácia não é qualquer comércio e tem que ter assistência à população
Alice Portugal ressalta que farmácia não é qualquer comércio e tem que ter assistência à populaçãoSegundo o projeto que está pronto para votação no Plenário, apenas farmácias, que manipulam e preparam medicamentos, seriam obrigadas a ter esse profissional, o que colocaria a população em risco, na opinião de parlamentares.
O Projeto de Lei 4385/94, do Senado, que torna obrigatória a presença de um farmacêutico nas farmácias, está pronto para ser votado no Plenário da Câmara dos Deputados, mas está gerando polêmica porque permite que, no caso de drogarias e ervanários, exerça a função um auxiliar de farmácia ou um prático com pelo menos dez anos de atividade profissional.
Para a coordenadora da Frente Parlamentar em Defesa da Assistência Farmacêutica, deputada Alice Portugal (PCdoB-BA), essa brecha para que pessoas sem formação exerçam o papel de farmacêutico coloca em risco a segurança da população. "Farmácia é coisa séria, não é qualquer comércio, não é pra se vender sandálias, bebidas alcoólicas e outras coisas que são comercializadas em farmácias brasileiras. Têm que ter controle sanitário e assistência à população", ressalta.
De acordo com definição da Agência Nacional de Vigilância Sanitária (Anvisa), farmácia “é o estabelecimento de manipulação de fórmulas magistrais e oficinais, de comércio de drogas, medicamentos, insumos farmacêuticos e produtos para saúde (correlatos)”. Já as drogarias não têm laboratório para preparação de fórmulas, pois apenas vendem medicamentos industrializados, enquanto os ervanários negociam plantas medicinais ou ervas em geral.
O coordenador da assessoria técnica do Conselho Federal de Farmácia, José Luiz Maldonado, lembrou que o projeto é de 1994, época em que havia uma carência muito grande de farmacêuticos no Brasil, e por isso previa a permissão de que, no caso da ausência desse profissional, a drogaria ou ervanário contasse com um técnico ou um prático.
No entanto, ele alerta para o perigo da falta de um profissional capaz de esclarecer as dúvidas dos pacientes. "Não é suficiente ter a oferta de medicamento se ele é incorretamente utilizado. Estamos sempre preocupados com o uso racional do medicamento de tal forma que tenha a salvaguarda de um profissional atrás do balcão que seja farmacêutico", afirma.
Lei orgânica
Relator do projeto na Comissão de Defesa do Consumidor, o deputado Ivan Valente (Psol-SP) apresentou um substitutivo que inclui as farmácias entre os serviços de atenção à saúde do Sistema Único de Saúde (SUS) e estabelece regras para o exercício e a fiscalização da atividade farmacêutica.
No texto apresentado, Valente determina que drogarias e ervanários tenham o mesmo tratamento dado às farmácias, com a exigência de presença de um farmacêutico durante todo o período de funcionamento. Para que os estabelecimentos já existentes se adequem às regras, ele prevê um prazo de transição de cinco anos, que poderá ser prorrogado por dois anos em municípios com menos de dez mil habitantes.
"É um retrocesso que no nosso País ainda não tenhamos uma lei orgânica da farmácia, uma assistência farmacêutica integral como direito do cidadão", destacou, acrescentando que nesses locais é possível colher dados estatísticos sobre a saúde da população, o que pode ajudar a traçar diretrizes para as políticas públicas.
Ivan Valente afirmou ainda que, no caso de municípios pequenos, o governo deverá ser responsável por fornecer assistência farmacêutica para a população.
Tramitação
O projeto recebeu duas emendas no Plenário, que foram rejeitadas pelas comissões de Defesa do Consumidor; de Seguridade Social e Família; de Trabalho, de Administração e Serviço Público; e de Constituição e Justiça e de Cidadania.
Uma das emendas permitia que armazéns, depósitos e mercearias comercializassem produtos farmacêuticos de venda livre ou sem exigência de prescrição médica em regiões ribeirinhas e de baixa densidade populacional. A outra dispensava os fabricantes de remédio de incluir mensagens esclarecedoras sobre os produtos em suas propagandas, responsabilidade que passava para a Agência Nacional de Vigilância Sanitária (Anvisa).
Agora, a proposta está pronta novamente para ser votada pelo Plenário
Fonte: click News
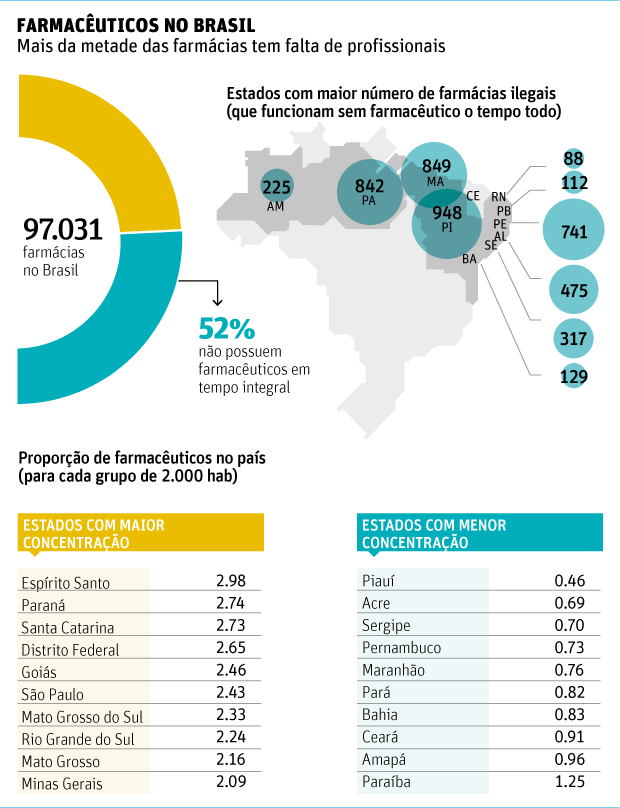
Faltam farmacêuticos em metade das farmácias do país, diz censo
CLÁUDIA COLLUCCI - DE SÃO PAULO
20/01/2014 02h00
Metade das 97 mil farmácias e drogarias do Brasil funciona
irregularmente, sem técnico responsável em horário integral. Na maioria,
a falta ocorre em certas horas do dia, mas 10% delas não têm
farmacêutico nunca.
Os números constam de um censo obtido com exclusividade pela Folha, que
será lançado hoje pelo ICTQ (instituto de pós graduação para
farmacêuticos). Lei de 1973 determina a presença do farmacêutico durante
todo o tempo de funcionamento da farmácia, sob pena de multas e até
interdição do local.
Entre as funções do farmacêutico estão conferir a receita do médico,
orientar o consumidor sobre o remédio e prescrever remédios que não
exijam receita médica.
"Em muitas farmácias, é o atendente que faz as vezes de farmacêutico.
Isso expõe a população a complicações em quadros clínicos de saúde e até
risco de morte", afirma Marcus Vinícius Andrade, que coordenou o
estudo.
Dos 1.923 usuários entrevistados, 54% não conseguem diferenciar o farmacêutico do atendente de balcão.
| Editoria de Arte/Folhapress | ||
 |
Para a Abrafarma (associação brasileira de farmácias)existe um déficit de ao menos 30 mil profissionais. Hoje há 180 mil farmacêuticos registrados no país, mas 30% não trabalham em farmácias. Atuam em laboratórios e unidades de saúde, por exemplo.
"Muitas querem contratar, mas não encontram profissionais. Tem rede reduzindo as unidades 24h porque não acha farmacêutico", diz Sérgio Mena Barreto, presidente da Abrafarma.
Já o CFF (Conselho Federal de Farmácia) nega que haja falta de profissionais e afirma que o problema é o excesso de farmácias, muitas delas funcionando de forma ilegal.
"O Brasil tem cinco vezes mais farmácia do que o necessário. Qualquer baiuca se intitula farmácia, coloca uma prateleira e começa a vender remédio", diz Walter Jorge João, presidente do CFF.
Segundo ele, há farmacêuticos suficientes e, nos próximos quatro anos, as escolas devem formar mais 80 mil.
João diz que em muitas farmácias tidas como irregulares a ausência do farmacêutico é temporária. "Saiu para almoçar ou está férias e a farmácia não conseguiu repor", explica ele, que contesta os resultados da pesquisa. "Será que eles foram em todas as farmácias e em todos os horários para concluir isso?"
O ICTQ diz ter cruzado dados de todos os conselhos de farmácia do país com os de farmácias e drogarias. Além disso, entrevistou 1.923 usuários e 2.331 profissionais.
Para Pedro Eduardo Menegasso, presidente do Conselho Regional de Farmácia de São Paulo, o déficit é causado pela má distribuição dos farmacêuticos. "É o que acontece no caso dos médicos. Há uma concentração de profissionais no Sul e no Sudeste."
Em alguns Estados, a falta de farmacêuticos chegou ao Ministério Público. Na Paraíba, onde 112 farmácias funcionam sem o profissional, algumas delas se livraram de punição porque provaram que não preenchem as vagas por falta de interessados.
"Fechar farmácias por falta de farmacêutico não é um bom negócio para a
população, sobretudo nas cidades menores", diz Mena Barreto.
Fonte: Folha de São Paulo
Fonte: Folha de São Paulo
sexta-feira, 17 de janeiro de 2014
Anvisa propõe mudanças no mercado de medicamentos similares
15/08/2002 - 17h27
Brasília, 15 (Agência Brasil - ABr) -
A Agência Nacional de Vigilância Sanitária (Anvisa) propõe novas regras
para o mercado de medicamentos. As principais dizem respeito ao
segmento dos medicamentos similares e estão contidas na Consulta Pública
nº 62, publicada ontem no Diário Oficial da União. A resolução
resultante da consulta pública substituirá a Instrução Normativa 01/94,
que não atende mais às novas tecnologias e conceitos do mercado
farmacêutico, como medicamentos genéricos e patentes, que surgiram
depois de 1994.
Uma das principais mudanças propostas é a obrigatoriedade da realização dos testes de biodisponibilidade para os similares, ensaios que comprovarão se o produto têm a mesma eficácia, segurança e toxicidade do medicamento de referência ao qual se reportam, a exemplo do que hoje se tem para os medicamentos genéricos, com a exigência para estes, de ensaios de bioequivalência. A realização dos testes não implicará na possibilidade de troca do similar pelo farmacêutico no balcão da farmácia em lugar do medicamento receitado pelo médico. De acordo com a Lei nº 9.787/99, o farmacêutico somente poderá trocar o medicamento de referência receitado pelo médico por um genérico.
Caso não consiga comprovar compatibilidade entre um similar e seu respectivo referência, o laboratório deverá demonstrar que a diferença encontrada em seu medicamento é positiva, tendo então que ser submetido aos critérios e às exigências relativas ao segmento de produtos novos. Os pedidos de registro de similares já solicitados terão prazo de um ano para se adequar à legislação.
Quando entrar em vigor, a nova resolução punirá as empresas que não cumprirem as determinações, de acordo com a Lei nº 6.437/77, que prevê desde notificação até multas de R$ 2 mil a R$ 1,5 milhão.
Os interessados têm até 27 de setembro para apresentar críticas e sugestões à proposta no endereço: Agência Nacional de Vigilância Sanitária, SEPN 515, Bloco "B" Ed. Ômega, Asa Norte, Brasília-DF, CEP 70.770.502 ou Fax: (61) 448-1489 ou E-mail: ggsps@anvisa.gov.br. Terminado o prazo, a Anvisa promoverá seminário para discutir com entidades interessadas no assunto a consolidação do texto final.
Fonte: Agencia Brasil
Uma das principais mudanças propostas é a obrigatoriedade da realização dos testes de biodisponibilidade para os similares, ensaios que comprovarão se o produto têm a mesma eficácia, segurança e toxicidade do medicamento de referência ao qual se reportam, a exemplo do que hoje se tem para os medicamentos genéricos, com a exigência para estes, de ensaios de bioequivalência. A realização dos testes não implicará na possibilidade de troca do similar pelo farmacêutico no balcão da farmácia em lugar do medicamento receitado pelo médico. De acordo com a Lei nº 9.787/99, o farmacêutico somente poderá trocar o medicamento de referência receitado pelo médico por um genérico.
Caso não consiga comprovar compatibilidade entre um similar e seu respectivo referência, o laboratório deverá demonstrar que a diferença encontrada em seu medicamento é positiva, tendo então que ser submetido aos critérios e às exigências relativas ao segmento de produtos novos. Os pedidos de registro de similares já solicitados terão prazo de um ano para se adequar à legislação.
Quando entrar em vigor, a nova resolução punirá as empresas que não cumprirem as determinações, de acordo com a Lei nº 6.437/77, que prevê desde notificação até multas de R$ 2 mil a R$ 1,5 milhão.
Os interessados têm até 27 de setembro para apresentar críticas e sugestões à proposta no endereço: Agência Nacional de Vigilância Sanitária, SEPN 515, Bloco "B" Ed. Ômega, Asa Norte, Brasília-DF, CEP 70.770.502 ou Fax: (61) 448-1489 ou E-mail: ggsps@anvisa.gov.br. Terminado o prazo, a Anvisa promoverá seminário para discutir com entidades interessadas no assunto a consolidação do texto final.
Fonte: Agencia Brasil
Consulta pública sobre medicamentos similares deve começar em sete dias
17/01/2014 - 11h18
Paula Laboissière
Repórter da Agência Brasil
 Brasília - A Agência Nacional de Vigilância Sanitária (Anvisa) publicou hoje (17) no Diário Oficial da União
consulta pública que propõe a inclusão de medicamentos similares como
mais uma opção aos medicamentos de referência ou de marca, como já
ocorre com os genéricos.
Brasília - A Agência Nacional de Vigilância Sanitária (Anvisa) publicou hoje (17) no Diário Oficial da União
consulta pública que propõe a inclusão de medicamentos similares como
mais uma opção aos medicamentos de referência ou de marca, como já
ocorre com os genéricos.
A consulta pública deve ser aberta em sete dias e será mantida por um período de 30 dias. A expectativa do governo é que a proposta, se aprovada, amplie a oferta de remédios a preços mais baratos para o consumidor. Ainda de acordo com o texto, os medicamentos similares deverão incluir em suas embalagens o símbolo EQ, que significa equivalente.
A proposta da agência é que uma mesma prescrição médica, que atualmente permite a compra de um remédio de marca ou de um genérico, permita também a compra do remédio similar, que contém os mesmos princípios ativos, a mesma concentração e a mesma posologia que o de referência.
Ontem (16), o ministro da Saúde, Alexandre Padilha, disse que vai defender, na Câmara de Medicamentos, que as mesmas regras adotadas para remédios genéricos passem a valer para os similares – incluindo uma redução de, pelo menos, 35% no preço em relação aos de marca.
Dados da pasta indicam que, em 2012, em quantidade comercializada, os medicamentos similares representaram 24,8% do mercado nacional. Os genéricos ficaram com 37,1% e os de referência, com 23,2%.
Edição: Talita Cavalcante
Todo o conteúdo deste site está publicado sob a Licença Creative Commons Atribuição 3.0 Brasil. Para reproduzir as matérias é necessário apenas dar crédito à Agência Brasil
Repórter da Agência Brasil
 Brasília - A Agência Nacional de Vigilância Sanitária (Anvisa) publicou hoje (17) no Diário Oficial da União
consulta pública que propõe a inclusão de medicamentos similares como
mais uma opção aos medicamentos de referência ou de marca, como já
ocorre com os genéricos.
Brasília - A Agência Nacional de Vigilância Sanitária (Anvisa) publicou hoje (17) no Diário Oficial da União
consulta pública que propõe a inclusão de medicamentos similares como
mais uma opção aos medicamentos de referência ou de marca, como já
ocorre com os genéricos.A consulta pública deve ser aberta em sete dias e será mantida por um período de 30 dias. A expectativa do governo é que a proposta, se aprovada, amplie a oferta de remédios a preços mais baratos para o consumidor. Ainda de acordo com o texto, os medicamentos similares deverão incluir em suas embalagens o símbolo EQ, que significa equivalente.
A proposta da agência é que uma mesma prescrição médica, que atualmente permite a compra de um remédio de marca ou de um genérico, permita também a compra do remédio similar, que contém os mesmos princípios ativos, a mesma concentração e a mesma posologia que o de referência.
Ontem (16), o ministro da Saúde, Alexandre Padilha, disse que vai defender, na Câmara de Medicamentos, que as mesmas regras adotadas para remédios genéricos passem a valer para os similares – incluindo uma redução de, pelo menos, 35% no preço em relação aos de marca.
Dados da pasta indicam que, em 2012, em quantidade comercializada, os medicamentos similares representaram 24,8% do mercado nacional. Os genéricos ficaram com 37,1% e os de referência, com 23,2%.
Edição: Talita Cavalcante
Todo o conteúdo deste site está publicado sob a Licença Creative Commons Atribuição 3.0 Brasil. Para reproduzir as matérias é necessário apenas dar crédito à Agência Brasil
Fonte: Agencia Brasil
quinta-feira, 16 de janeiro de 2014
Programa mais médicos e a escrituração dos produtos controlados.
Atendimento e dispensação de receitas prescritas por profissionais do programa Mais Médicos
A
RDC nº 52/2013 estabelece que o número de Registro Único, emitido pelo
Ministério da Saúde, nos termos do parágrafo 3º do art. 16 da Lei nº
12.871/2013, é informação apta a substituir o número da inscrição no
Conselho Regional de Medicina (CRM) em notificações de receitas,
receitas de controle especial, prescrições de antimicrobianos ou em
quaisquer outras situações onde tal número de inscrição seja exigido
pelas normas sanitárias.
Com
relação à escrituração eletrônica de medicamentos, foi realizada
adaptação no SNGPC para que possa ser registrado também o número de
Registro do Ministério da Saúde, além dos já permitidos números de CRM,
CRO e CRMV. Desta forma, as farmácias e drogarias devem escriturar as
receitas prescritas pelos profissionais estrangeiros legalmente
habilitados para atuar no Brasil e que possuam seu número de inscrição
no Programa Mais Médicos, através na identificação do RMS (Registro
Ministério da Saúde).
Lembramos
que as adaptações no sistema informatizado interno de cada
estabelecimento devem ser realizadas pelos desenvolvedores. Foi incluído
no schema XML o tipo simples (simple type) denominado RMS que segue as
mesmas regras do tipo CRM já existente, ou seja, permite a dispensação
de medicamentos para uso humano.
Fonte: Sistema Nacional de Gerenciamento de Produtos Controlados – SNGPC
04/12/2013
divulgação: Sincofarma MG
quarta-feira, 15 de janeiro de 2014
Lei que autoriza PF investigar remédios falsificados é publicada no Diário Oficial
Polícia Federal também investigará esta prática ilícita
Foi publicada no Diário Oficial da União desta quarta-feira (18), lei aprovada pela presidenta Dilma Rousseff que inclui a falsificação e a adulteração de remédios entre os crimes de repercussão interestadual ou internacional. Além ser investigado pela Polícia Civil, este tipo de prática ilícita será alvo também da PF (Polícia Federal).
A Lei 12.894 inclui a “falsificação, corrupção, adulteração ou alteração de produto destinado a fins terapêuticos ou medicinais e venda, inclusive pela internet, depósito ou distribuição do produto falsificado, corrompido, adulterado ou alterado” entre os crimes que, por excederem à atuação das polícias estaduais, exige “repressão uniforme”.
A nova medida acrescenta um inciso à Lei 10.446 de 2002, que já previa o trabalho da PF na investigação de outros crimes de repercussão interestadual ou internacional como sequestro, cárcere privado, extorsão, formação de cartel, violações a direitos humanos ou furtos, roubos ou recepção de cargas,“sem prejuízo da responsabilidade de outros órgãos de segurança pública, em especial das Polícias Militares e Civis dos Estados”.
Fonte: Agência Brasil
Farmácias populares
Donos de farmácias
populares – que oferecem medicamentos com desconto de até 90%, por meio
de subsídio do governo federal – estão tendo problemas administrativos e
até judiciais por não cumprirem a Portaria 971, do Ministério da Saúde.
Ela estabelece a obrigatoriedade de arquivamento dos cupons fiscais,
dos cupons vinculados e das receitas médicas por períodos de até cinco
anos para apresentação sempre que for necessário ou solicitado por
auditoria. O advogado Leonardo Bezerra Cunha explica que, apesar da
obrigatoriedade, as farmácias e drogarias populares muitas vezes não
armazenam o material solicitado. Segundo relatório do TCU de 2010, isso
acontece por falta de treinamento e profissionais. Leonardo alerta que a
empresa nessa situação pode ser punida até com descredenciamento do MS.
Ministério da Saúde oferece capacitação para farmacêuticos
segunda, 13 de janeiro de 2014 às 18h57
O objetivo da
capacitação é qualificar técnica e humanisticamente o profissional
farmacêutico para atuar na Atenção Primária em Saúde

Proposta de trabalho é baseada na problematização de situações cotidianas do farmacêutico. (Foto: Reprodução/Internet.)
Estão abertas as inscrições para o curso “Farmacêuticos na Atenção Primária à Saúde: Trabalhando em Rede”, fruto de uma parceria entre Ministério da Saúde, por meio do Programa Nacional de Qualificação da Assistência Farmacêutica no âmbito do SUS (Qualifar SUS), e a Faculdade de Farmácia da Universidade Federal do Rio Grande do Sul (UFRGS).
O objetivo da capacitação é qualificar técnica e humanisticamente o profissional farmacêutico para atuar na Atenção Primária em Saúde, desenvolvendo com competência as atividades de núcleo e de campo, pautadas nos princípios do Sistema Único de Saúde (SUS). O curso é gratuito e envolve etapa presencial e a distância. A proposta de trabalho é baseada na problematização de situações cotidianas do profissional farmacêutico que se ramificarão ao longo dos módulos. A carga horária total do curso é de 350 horas e 200 vagas serão oferecidas nesta edição.
As inscrições estão abertas até o dia 31 de janeiro. Para se inscrever, clique aqui.
Fonte: Com informações do CFF.
Divulgação: CRF-MS
FDA: Acetaminophen doses over 325 mg might lead to liver damage
By Holly Yan, CNN
January 15, 2014 -- Updated 1627 GMT (0027 HKT)

Taking more than the recommended dose of a pain reliever with acetaminophen can lead to liver damage in healthy people.
(CNN) -- You're in pain after surgery, and your
doctor prescribes you Vicodin, or maybe Percocet. But when you get home,
the pain hasn't subsided and you decide to pop some Extra Strength
Tylenol.
Unknowingly, you may have just taken more of the drug acetaminophen than is safe.
Acetaminophen is often
used in pain medications with opioids such as oxycodone (Percocet),
hydrocodone (Vicodin) and codeine (Tylenol with Codeine). These are
called combination drugs, and the Food and Drug Administration is asking
doctors to stop prescribing those that have more than 325 mg of
acetaminophen per dose.
The FDA says no data show that taking more than that amount provides enough benefit to outweigh the risk of liver damage.
"Many consumers are often
unaware that many products (both prescription and OTC) contain
acetaminophen, making it easy to accidentally take too much," the FDA
said in a statement Tuesday.
The warning does not
apply to over-the-counter drugs such as Tylenol, which contains
acetaminophen. The FDA said it will address over-the-counter products in
another regulatory action.
In 2011, the FDA asked
manufacturers to limit the amount of acetaminophen in prescription
combination drugs to 325 mg per capsule or tablet by January 2014. While
more than half of the manufacturers agreed, some combination drugs with
higher amounts of acetaminophen remain on the market.
The federal agency says
it plans to start the process of withdrawing approval of prescription
combination drugs from manufacturers that have not complied.
Health risks
"Acetaminophen overdose is one of the most common poisonings worldwide," according to the National Institutes of Health.
Taking too much of this pain reliever can lead to liver failure or death.
The FDA has set the
recommended maximum for adults at 4,000 milligrams per day. It's easier
to reach this limit than you might think; one gel tablet of Extra
Strength Tylenol, for example, contains 500 mg.
Consumers should not
take more than the prescribed dose of any medication that contains
acetaminophen, according to the FDA, and should avoid taking more than
one acetaminophen product at a time. Drinking alcohol while taking
acetaminophen also puts you at risk.
To find out if your
medications contain acetaminophen, read the drug label or the list of
ingredients in the patient information leaflet that came with your
prescription. Look for the word "acetaminophen" or the letters "APAP,"
an abbreviation sometimes used for the drug. If you are still unsure,
contact your doctor or pharmacist.
Acetaminophen may also
cause serious skin reactions in some people. According to the FDA, the
skin reactions are rare but can be deadly. These conditions can cause
blisters, serious rashes, reddening of the skin and the detachment of
the upper surface of the skin, the epidermis.
Anyone who develops
these types of conditions after using acetaminophen should stop taking
the product immediately and visit a doctor or emergency room.
CNN's Jacque Wilson, Saundra Young and Val Willingham contributed to this report.
Fonte: CNN
terça-feira, 14 de janeiro de 2014
Controle ANVISA - GS1 rastreará medicamentos
Jéssica Mello // terça, 14/01/2014 10:01
A Agência Nacional de Vigilância Sanitária (Anvisa) escolheu a tecnologia de código de barras bidimensional GS1 DataMatrix, para rastrear os medicamentos desde a fabricação até chegar à farmácia. As regras do Sistema Nacional de Controle de Medicamentos foram aprovadas pela agência e tem o prazo máximo de três anos para entrar em vigor.
Com o código do produto, é possível recuperar informações históricas e
geográficas sobre o caminho percorrido pelos remédios a fim de evitar o
contrabando e as falsificações. Afinal, segundo a Anvisa, 20% dos
medicamentos vendidos no Brasil são falsos.
O DataMatrix será responsável pela captura, armazenamento e
transmissão eletrônica dos dados necessários para acompanhar o trajeto.
Ao contrário do código de barras comum, que contém apenas o número de
identificação do produto, o bidimensional armazena informações
variáveis como lote, validade e número serial.
Todas essas informações são chamadas de Identificador Único de Medicamento (IUM).
O código vai permitir identificar fontes de desvios de qualidade e reduzir os custos logísticos dos fabricantes.
“A preocupação com a segurança do paciente e a autenticidade dos
medicamentos se torna cada vez mais presente em todo o mundo, e a
rastreabilidade é uma ferramenta essencial para ajudar a enfrentar esta
situação. A identificação única do item por meio do código de barras é a
base do processo”, destaca o presidente da GS1 Brasil, João Carlos de
Oliveira.
O mercado também adicionará nesta combinação o GTIN, número do código de barras do produto, já utilizado anteriormente.
A GS1 Brasil, entidade de apoio a tecnologias de automação no país,
comemorou seus trinta anos no país em novembro. Em 2014, mudará de sede
em São Paulo. O novo local terá 350 metros quadrados e contará com um
Centro de Inovação e Tecnologia.
Atualmente, a GS1 conta com 57 mil empresas associadas, que atuam em
cerca de 22 setores, desde indústria, varejo, passando por saúde e
setores públicos. Em suas ações, cerca de 15 mil pessoas são treinadas
atualmente no uso de tecnologias de automação.
Fonte: Baguete
segunda-feira, 6 de janeiro de 2014
O potencial do mercado farmacêutico na América Latina
Os gastos anuais com saúde são de 180 mil milhões de dólares e o investimento total na região é de 2,9% do PIB
Antes
de falar sobre qualquer assunto da América Latina é preciso recordar:
este conjunto de países que representa perto de 600 milhões de
habitantes - que partilham vínculos geográficos, linguísticos, culturais
e comportamentais - registou, entre 2000 e 2012, um crescimento
económico médio anual de 5%, tem uma população jovem e com uma taxa de
desigualdades sociais cada vez menor, classes médias em plena expansão e
com maior poder de consumo e tem conhecido um desenvolvimento notável
em termos de segurança, modernização das estruturas produtivas e
amadurecimento das instituições democráticas.
Tendo estes pontos bem assentes, podemos focar-nos numa das áreas que mais potencialidade de negócios oferecem às empresas portuguesas: o sector farmacêutico.
O mercado farmacêutico na América Latina estava avaliado em 2012 em 63 mil milhões de dólares. Entre 2009 e 2019, estima-se que o consumo per capita passará de 77 para 129 dólares. Os gastos com saúde são de 180 mil milhões de dólares anuais e o investimento total na região é de 2,9% do PIB. A expectativa média de vida é de 75 anos e as vendas totais de produtos farmacêuticos totalizaram, no último ano, 50 mil milhões de dólares.
É também verdade que este mercado apresenta dificuldades e perguntas difíceis de responder, sobretudo no que diz respeito à heterogeneidade legislativa: como se faz a certificação de um produto, como se faz a sua adaptação aos climas tropicais, se Portugal está incluído nos países de referência de cada Estado, se existem MOU com as autoridades oficiais de cada país, quais são os procedimentos regulamentares para introdução de medicamentos no mercado, qual a legislação que regulamenta a comercialização e a importação de dispositivos médicos, qual a política fiscal e alfandegária, entre tantas outras. Parece uma tarefa hercúlea mas nenhuma destas questões tem impedido as farmacêuticas portuguesas de conquistarem estes mercados, com tal êxito que hoje em dia já se tornaram fundamentais para a sua facturação.
No Fórum Empresarial "Medicamento e Produtos de Saúde", organizado recentemente pelo IPDAL e pela Ordem dos Farmacêuticos, a esmagadora maioria das empresas presentes já exportava ou inclusivamente já tinha operações montadas no terreno, em vários países da América Latina.
Fonte: Jornal i
Tendo estes pontos bem assentes, podemos focar-nos numa das áreas que mais potencialidade de negócios oferecem às empresas portuguesas: o sector farmacêutico.
O mercado farmacêutico na América Latina estava avaliado em 2012 em 63 mil milhões de dólares. Entre 2009 e 2019, estima-se que o consumo per capita passará de 77 para 129 dólares. Os gastos com saúde são de 180 mil milhões de dólares anuais e o investimento total na região é de 2,9% do PIB. A expectativa média de vida é de 75 anos e as vendas totais de produtos farmacêuticos totalizaram, no último ano, 50 mil milhões de dólares.
É também verdade que este mercado apresenta dificuldades e perguntas difíceis de responder, sobretudo no que diz respeito à heterogeneidade legislativa: como se faz a certificação de um produto, como se faz a sua adaptação aos climas tropicais, se Portugal está incluído nos países de referência de cada Estado, se existem MOU com as autoridades oficiais de cada país, quais são os procedimentos regulamentares para introdução de medicamentos no mercado, qual a legislação que regulamenta a comercialização e a importação de dispositivos médicos, qual a política fiscal e alfandegária, entre tantas outras. Parece uma tarefa hercúlea mas nenhuma destas questões tem impedido as farmacêuticas portuguesas de conquistarem estes mercados, com tal êxito que hoje em dia já se tornaram fundamentais para a sua facturação.
No Fórum Empresarial "Medicamento e Produtos de Saúde", organizado recentemente pelo IPDAL e pela Ordem dos Farmacêuticos, a esmagadora maioria das empresas presentes já exportava ou inclusivamente já tinha operações montadas no terreno, em vários países da América Latina.
Estiveram
reunidas as 14 principais farmacêuticas nacionais com os embaixadores
da América Latina acreditados em Portugal numa sessão de esclarecimento
mútuo sobre as oportunidades que cada um oferece. Nas palavras do
presidente da AICEP, que encerrou os trabalhos, vão ser as empresas que
representam este cluster, que, por estarem a lograr conquistas e
crescimento em contraciclo com o resto da economia, irão ajudar o país a
dar a volta à situação em que se encontra actualmente. Para Pedro Reis,
o IPDAL e a Ordem dos Farmacêuticos conseguiram reunir "duas
prioridades do governo de Portugal: a América Latina e a indústria
farmacêutica".
Secretário-geral do Instituto para a Promoção e Desenvolvimento da América Latina
Secretário-geral do Instituto para a Promoção e Desenvolvimento da América Latina
Fonte: Jornal i
FDA: aprovação de medicamentos inovadores diminuiu em 2013
06/01/2014 - 09:39

A FDA (entidade que regula os medicamentos nos EUA) aprovou 27 medicamentos inovadores nem 2013, menos 39 que em 2012, avança a Associated Press, citada pela ABC News.
Apesar do decréscimo, a entidade reguladora norte-americana diz que o número de aprovações registadas no ano passado está em linha com a tendência histórica. Em média, a FDA aprovou 29 medicamentos inovadores por ano, nos últimos cinco anos.
Alguns analistas consideram que a descida verificada em 2013 também se deve ao facto de terem sido submetidos menos medicamentos para aprovação.
Segundo uma apresentação feita pela FDA a executivos da Indústria farmacêutica no mês passado, a entidade reguladora recebeu em 2013 pelo menos 32 pedidos para medicamentos inovadores, abaixo dos 41 que recebeu em 2012. Normalmente a FDA analisa os pedidos num período de seis a dez meses.
"Penso que isto espelhe um mau trabalho por parte da FDA, mas sim o número de pedidos que tem para analisar", disse Ira Loss, que se dedica ao sector farmacêutico na Washington Analysis.
Há pelo menos 25 pedidos de aprovação para medicamentos inovadores pendentes na FDA para 2014, sendo esperados ainda mais, de acordo com a Washington Analysis.
Divulgação: RCM Pharma
Fonte: Associated Press (AP)/ABC News
http://abcnews.go.com/Health/wireStory/drug-approvals-fda-declined-2013-21398584
Assinar:
Comentários (Atom)
